

DEKRA CE-certificering
Wilt u uw medische apparatuur certificeren om te voldoen aan de relevante wet- en regelgeving?
DEKRA CE-certificering
Wilt u uw medische apparatuur certificeren om te voldoen aan de relevante wet- en regelgeving?
IVDR Notified Body voor verplichte beoordeling
Regel uw certificaten via een IVDR Notified Body
Wilt u een medisch hulpmiddel voor in-vitrodiagnostiek op de Europese markt brengen? Dan is een CE-markering vereist. CE-markering voor in-vitrodiagnostische (IVD) producten toont aan dat er voldaan wordt aan de meest recente regelgeving: In Vitro Diagnostic Regulation (IVDR) 2017/746. Vaak heeft u hiervoor een beoordeling nodig van een notified body. DEKRA Certification B.V. kan als notified body beoordelen of uw product voldoet aan de IVDR. Tip: wees op tijd met het starten van uw aanvraag voor CE-markering van uw device onder de IVDR.
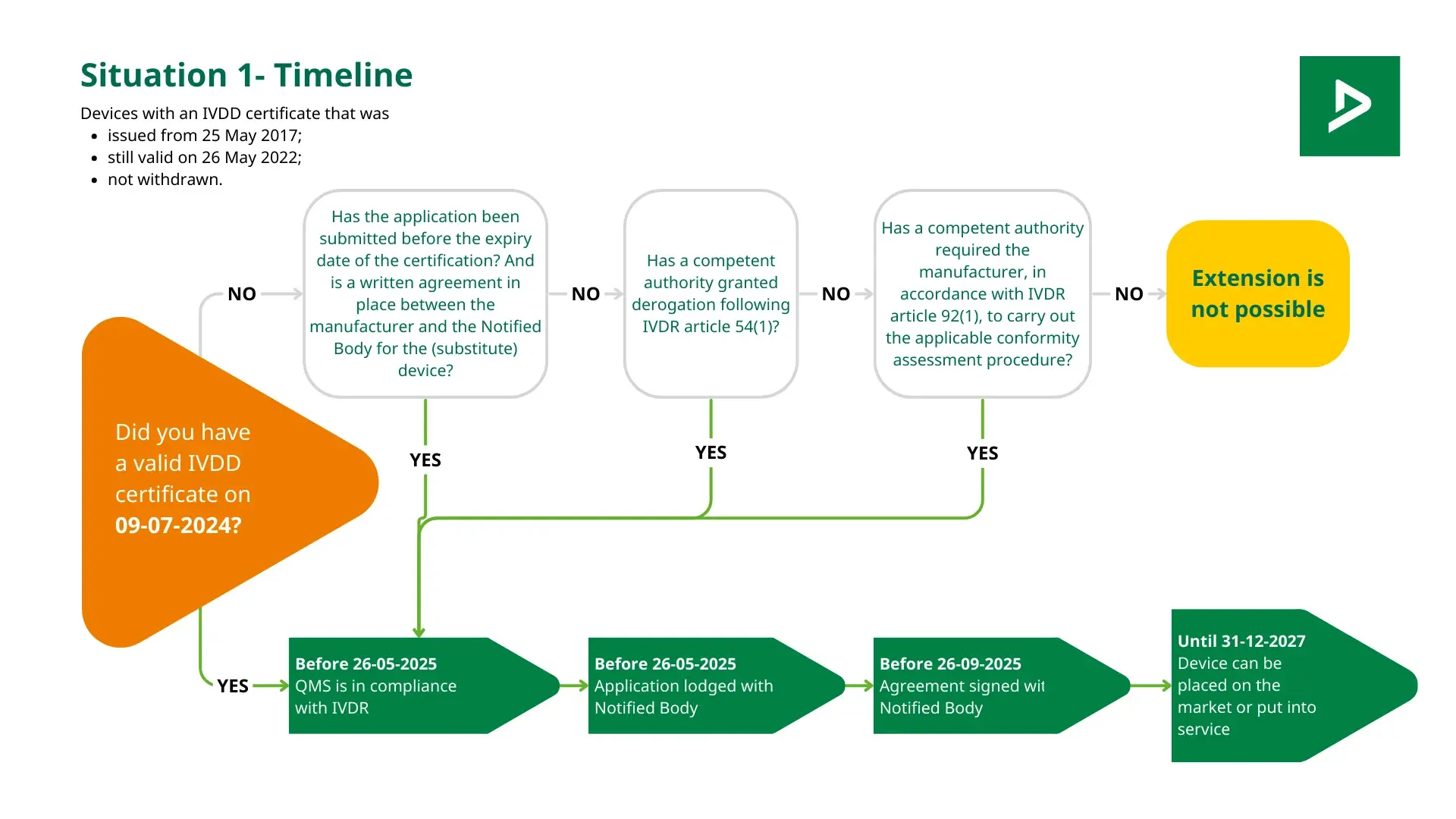
Certificering onder IVDR: Wat moet u weten?
Valt uw in-vitrodiagnostische product in klasse A steriel, B, C of D? En wilt u hiermee de Europese markt op? Dan bent u nu verplicht om een notified body in te schakelen voor de certificering van uw product. De nieuwe regelgeving In Vitro Diagnostic Regulation (IVDR) 2017/746 is sinds 2022 van kracht en verplicht voor alle IVD-producten na de vastgestelde overgangsperiode.

Wat is een CE-certificering voor medische hulpmiddelen?
De CE-markering (Conformité Européene) is de verklaring van de fabrikant dat een product voldoet aan de relevante voorschriften en normen. Hieronder vallen eisen op het gebied van veiligheid, gezondheid en milieubescherming. Alle medische hulpmiddelen die binnen de grenzen van de Europese markt worden gebracht, moeten voldoen aan de eisen die worden gesteld in de IVDR of de Wetgeving Medische Hulpmiddelen (MDR).
Wat is een notified body?
Een notified body is een organisatie die bevoegd is om de conformiteit van bepaalde producten te beoordelen voordat ze op de markt worden gebracht. Meestal wijst de overheid de notified bodies in haar land aan. DEKRA is als notified body aangewezen om de conformiteit van medische producten te beoordelen, volgens de regelgeving zoals beschreven in de IVDR en MDR.
Wanneer heeft u een notified body nodig voor CE IVDR-certificering?
Vallen uw in-vitrodiagnostieken in klasse A steriel, B, C of D van de IVDR? Dan is het verplicht om uw producten te laten certificeren via een notified body als u de Europese markt wilt betreden.
Wat zijn de vervolgstappen voor een IVDR-beoordeling?
Bent u geïnteresseerd in de certificeringservice die DEKRA biedt? Dien nu uw aanvraag in. Hoe eerder, hoe beter. Wanneer wij de gevraagde IVDR-diensten kunnen bieden, ontvangt u van ons een offerte. DEKRA's notified body toetst uw product tegen de IVDR-eisen met een:
- een off-site beoordeling van uw technisch dossier;
- een on-site kwaliteit managementsysteem (QMS) audit.
Is de uitkomst van de review van het technisch dossier en de audit positief? Dan verkrijgt u een CE-certificaat voor de betreffende producten. Houd er rekening mee dat dit proces, vanaf het ontvangen van een offerte tot aan de goedkeuring van het CE-certificaat, een lange tijd in beslag kan nemen; anderhalf jaar is geen uitzondering. De doorlooptijd is sterk afhankelijk van de kwaliteit van uw technisch- en conformiteitsbewijs.

Heeft uw product een elektrisch component of draadloze verbinding?
In dat geval moet uw product eerst getest worden op veiligheidsaspecten. Bijvoorbeeld op elektrische veiligheid, elektrisch magnetische comptabiliteit (EMC) of draadloze technologieën. Het testen gebeurt door een daarvoor geaccrediteerde testlaboratorium, zoals DEKRA Product Testing. De testen en de eventueel bijbehorende certificaten zijn onderdeel van het beoordelingsproces van de notified body. DEKRA notified body accepteert testen en certificaten van DEKRA Product Testing, of van een ander geaccrediteerd testlaboratorium. Lees hier meer over het testen van medische hulpmiddelen door DEKRA Product Testing.
Waarom nu uw IVDR-aanvraag indienen bij onze notified body?
Nogmaals: wij drukken u op het hart om uw aanvraag op tijd in te dienen. De flexibiliteit van de notified body voor het plannen van beoordelingen en audits is beperkt. Dit komt door de hoge werklast die de EU IVDR-transitie met zich meebrengt. Bovendien loopt de transitieperiode steeds sneller af.
Start uw aanvraag
Vraag een offerte aan of een gesprek met één van onze experts. Tijdens deze sessie heeft u de tijd om uw business case te bespreken en al uw vragen aan onze expert te stellen. Vul het onderstaande formulier in en we nemen zo snel mogelijk contact met u op om een afspraak te maken.

